Degré de dissociation
Définition du degré de dissociation
Il est noté α et représente la proportion de produit dissocié. Il s'écrit:
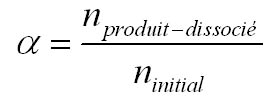
Il n'a pas d'unité et peut s'exprimer en %.
Si α = 1 la réaction est totale
Exemple: soit la réaction AH2 ![]() A2- + 2H+
A2- + 2H+
| AH2 |
A2- | + 2H+ | |
| t=0 | C | 0 | 0 |
| t | C-Cα | αC | 2αC |
Exercice sur le degré de dissociation
On place du PCl5 dans une enceinte qui se dissocie selon la réaction:
PCl5(g) ![]() PCl3(g) + Cl2(g)
PCl3(g) + Cl2(g)
La pression initiale est P0. A l'équilibre, la pression se stabilise à P = 1,2 P0. Calculer le coefficient de dissociation de PCl5.
Réponse:
PCl5(g) 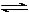 PCl3(g) + Cl2(g)
PCl3(g) + Cl2(g)
| AH2 |
A2- | + 2H+ | |
| t=0 | P0 | 0 | 0 |
| t | (1-α)P0 | αP0 | αP0 |
La pression à l'équilibre vaut 1,2 P0 d'où α = 0,2