La cellule électrochimique
Une cellule électrochimie est composée de 2 électrodes immergées dans des électrolytiques. La cellule est généralement compartimentée pour éviter que les solutions réagissent entre elles. Un pont salin permet de faire la jonction électrique.
La pile est un des modes de fonctionnement d'une cellule électrochimique qui illustre bien la séparation des électrolytes entourant chaque électrode.
Un voltmètre reliant les 2 électrodes permet de mesurer la différence de potentiel.
Schéma d'une cellule électrochimique
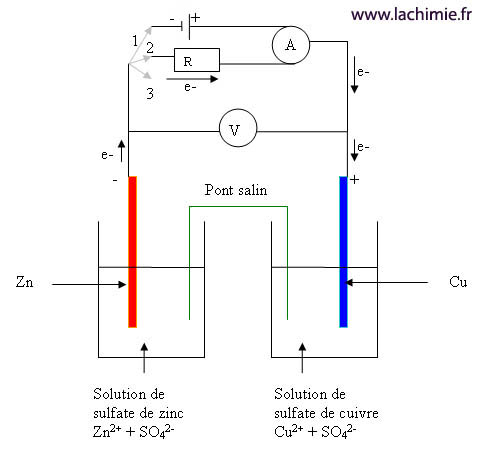
Dans cet exemple le sens de circulation des électrons est noté pour un fonctionnement en mode pile
3 modes de fonctionnement sont possibles selon la position du sélecteur ( 1,2 ou 3).
- en position 1 : la cellule fonctionne en électrolyse. Le sens du courant est inversé
- en position 2 : fonctionnement en pile
- en positon 3 : circuit ouvert : permet de mesurer la différence de potentiel entre les 2 électrodes
Important : La tension ne dépend pas du sens du courant. quelque soit le mode de fonctionnement, les signes aux bornes du voltmètre restent inchangé!
Cellules réversibles : une inversion de courant entraîne simplement le sens de la réaction chimique
Cellules irréversibles : une inversion de courant entraîne de nouvelles des réactions différentes à l'une ou au 2 électrodes.