Dosage par la méthode des ajouts dosés
Principe de la méthode des ajouts dosés
La méthode consiste à faire varier la concentration de l'analyte à doser de la solution en effectuant des ajouts de concentration connue de cet élément. On trace ensuite la courbe de calibration de l'aire en fonction de la concentration massique τe: A = f(τe) pour chaque ajout. On obtient une droite de relation générale A = a τe + b. Le rapport b/a est égal à la concentration en élément à doser ce qui revient à regarder graphiquement la valeur de la concentration massique lorsque l'aire A est égale à 0.
Calcul de la pente de la droite
Soit mi la masse inconnue d'analyte à doser contenu dans l'échantillon
soit me la masse d'analyte ajouté
A partir de la relation de la chromatographie, on peut écrire :
me + mi = KA
En remplaçant les masses par les concentrations massiques, on obtient :
τeV + τiV = KA
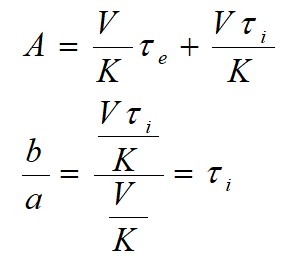 Lorsque A = 0, on obtient directement la concentration massique.
Lorsque A = 0, on obtient directement la concentration massique.
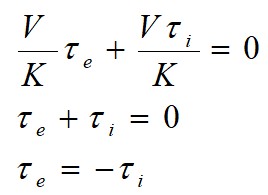
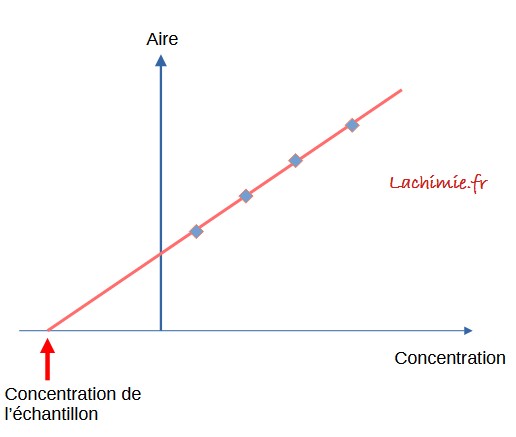
L'inconvénient de la méthode des ajouts dosés réside dans le fait qu'il faut disposer du produit pur pour effectuer l'ajout.
Cette méthode n'est pas propre à la chromatographie, elle peut être employée dans les autres méthodes d'analyses chimiques : photométrie de flamme, spectrométrie UV, etc...
Calcul sans droite d'étalonnage
On peut également utiliser la méthode sans courbe d'étalonnage mais cette méthode ne donne aucune information sur justesse de la mesure. Bien que plus rapide, elle n'est donc pas à conseillé.
Là aussi le dosage consiste à ajouter une masse m0 du composé à doser au mélange.
Pour chacun des composés l'on a :
Exemple : on cherche à déterminer la fraction massique x2 du mélange.
Soit :
- m0 : la masse de produit 2 ajouté au mélange
- A1 et A2: les aires respectives des composés 1 et 2 avant l’ajout de m0
- A’1 et A’2 : les aires respectives des composés 1 et 2 après l’ajout de m0
- m : la masse totale m = Smi
x2 = K2A2 / ∑ KiAi et x’2 = K2A’2 / ∑ KiA’i
d’où : x2 =x’2.A2/A’2 . ∑ KiA’i / ∑ KiAi
pour déterminer ∑ KiA’iet ∑ KiAi , on utilise un autre constituant (ici le 1)
∑ KiAi = K1A1/x1 et ∑ KiA’i = K1A’1/x’1
On en déduit x2 = A2A’1/A’2A1.x1/x’1.x’2
Il reste à éliminer x1 et x’1
x2 = m2/m
x’2 = (m2 +m0)/(m+m0)
x1 = m1/m
x’1= m1/(m+m0)
en en déduit que
x2 = (A2.A’1)/(A’2A1-A2A’1).m0/m
